Xét phản ứng phân hủy N2O5 ở 45oC
N2O5(g) → N2O4(g) + ½ O2(g)
Sau 184 giây đầu tiên, nồng độ của N2O4 là 0,25M. Tính tốc độ trung bình của phản ứng theo N2O4 trong khoảng thời gian trên.
Xét phản ứng phân hủy N2O5 trong dung môi CCl4 ở 45⁰:
N2O5 → N2O4 + ½ O2
Ban đầu nồng độ của N2O5 là 2,33M, sau 184 giây nồng độ của N2O5 là 2,08M.
Tốc độ trung bình của phản ứng tính theo N2O5 là
A.. 1,36.10-3 mol/(l.s)
B. 6,80.10-4 mol/(l.s)
C. 6,80.10-3 mol/(l.s)
D. 2,72.10-3 mol/(l.s)
Xét phản ứng phân hủy N2O5 trong dung môi CCl4 ở 45 độ C
N 2 O 5 → N 2 O 4 + 1 2 O 2
Ban đầu nồng độ của N2O5 là 2,33M, sau 184 giây nồng độ của N2O5 là 2,08M. Tốc độ trung bình của phản ứng tính theo N2O5 là
A. 2,72.10-3 mol/(l.s).
B. 1,36.10-3 mol/(l.s).
C. 6,80.10-3 mol/(l.s).
D. 6,80.10-4 mol/(l.s).
Xét phản ứng phân hủy N2O5 trong dung môi CCl4 ở 45oC : N2O5 ® N2O4 + 1 2 O2
Ban đầu nồng độ của N2O5 là 2,33M, sau 184 giây nồng độ của N2O5 là 2,08M. Tốc độ trung bình của phản ứng tính theo N2O5 là
A. 6,80.10-4 mol/(l.s)
B. 2,72.10-3 mol/(l.s).
C. 6,80.10-3 mol/(l.s).
D. 1,36.10-3 mol/(l.s).
Xét phân hủy N2O5 trong dung môi CCl4 ở 45oC: N2O5→N2O4 + 1/2O2. Ban đầu nồng độ của N2O5 là 2,33M, sau 184 giây nồng độ của N2O5 là 2,08M. Tốc độ trung bình của phản ứng tính theo N2O5 là:
A. 6,8.10-3mol/l.s
B. 2,72.10-3mol/l.s
C. 1,36.10-3mol/l.s
D. 6,8.10-4mol/l.s
Xét phản ứng phân hủy N2O5 trong dung môi CCl4 ở 45°C:
N 2 O 5 → N 2 O 4 + 1 / 2 O 2
Ban đầu nồng độ của N2O5 là 2,33 mol/lít, sau 184s nồng độ của N2O5 là 2,08 mol/lít. Tốc độ trung bình của phản ứng tính theo N2O5 là?
A. 6,80.10-4 mol/(l.s)
B. 2,72.10-2 mol/(l.s)
C. 1,36.10-2 mol/(l.s)
D. 6,80.10-2 mol/(l.s)
Bài tập ôn thi Hóa lý
Cho cân bằng N2O4 = 2NO2 ở 300C.
Giả sử ban đầu trong bình chỉ có N2O4 với áp suất là 760 mmHg. Khi phản ứng đạt cân bằng, áp suất trong bình là 800 mmHg.
a) Tính các loại hằng số cân bằng của phản ứng.
b) Xác định độ điện ly của N2O4 tại thời điểm áp suất trong bình là 780 mmHg.
c) Tính hiệu ứng nhiệt của phản ứng trên nếu biết hằng số cân bằng của phản ứng ở 250C là 1,15 mmHg.
Huy: có phải Kc bạn tính sai r k?
KC bạn ý tính đúng rồi mà!
Mình cũng tính ra vậy!
Cho phương trình hóa học của phản ứng: X + 2Y→Z+T. Ở thời điểm ban đầu, nồng độ của chất X là 0,01 mol/l. Sau 20 giây, nồng độ của chất X là 0,008 mol/l. Tốc độ trung bình của phản ứng tính theo chất X trong khoảng thời gian trên là
A. 4,0.10-4 mol/(l.s)
B. 7,5.10-4 mol/(l.s)
C. 1,0.10-4 mol/(l.s)
D. 5,0.10-4 mol/(l.s)
Chọn đáp án C.
Tốc độ trung bình của phản ứng tính theo chất X trong khoảng thời gian trên:
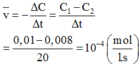
Cho phương trình hóa học của phản ứng: X + 2Y → Z + T. Ở thời điểm ban đầu, nồng độ của chất X là 0,01 mol/l. Sau 20 giây, nồng độ của chất X là 0,008 mol/l. Tốc độ trung bình của phản ứng tính theo chất X trong khoảng thời gian trên là
A. 5,0.10-4 mol/(l.s)
B. 1,0.10-4 mol/(l.s)
C. 4,0.10-4mol/(l.s)
D. 7,5.10-4 mol/(l.s)
Cho phương trình hóa học của phản ứng: X + 2Y → Z + T. Ở thời điểm ban đầu, nồng độ của chất X là 0,01 mol/l. Sau 20 giây, nồng độ của chất X là 0,008 mol/l. Tốc độ trung bình của phản ứng tính theo chất X trong khoảng thời gian trên là
A. 4 , 0 . 10 - 4 m o l / ( l . s )
B. 7 , 5 . 10 - 4 m o l / ( l . s )
C. 1 , 0 . 10 - 4 m o l / ( l . s )
D. 5 , 0 . 10 - 4 m o l / ( l . s )
Cho phương trình hóa học của phản ứng: X + 2 Y → Z + T Ở thời điểm ban đầu, nồng độ của chất X là 0,01 mol/l. Sau 20 giây, nồng độ của chất X là 0,008 mol/l. Tốc độ trung bình của phản ứng tính theo chất X trong khoảng thời gian trên là
A. 4,0.10-4 mol/(l.s).
B. 7,5.10-4 mol/(l.s).
C. 1,0.10-4 mol/(l.s).
D. 5,0.10-4 mol/(l.s).